序論
世界中の研究者たちが、SARS-Cov-2と呼ばれる新型コロナウイルスと戦うことの出来る可能性を持ったワクチンと薬剤を開発しようとして、競争しています。現在、一つの研究者たちのグループによって新しい発見がなされ、コロナウイルスが人間の細胞の中に侵入する際に用いる一つの重要なタンパク質の分子構造が解明されました。このことよって、ワクチン開発のための扉が開く可能性があります。
以前行われた研究によって、コロナウイルスはいわゆる「スパイク」タンパク質を介して細胞内に侵入することが分かっていましたが、このタンパク質は、コロナウイルスの種類によって、それぞれ異なる形をとっているのです。上級研究員であり、テキサス大学オースティン校の分子生物科学の准教授でもあるジェイソン・マクレラン(Jason McLellan)は、SARS-Cov-2のスパイクタンパク質の形状を解明することが、ウイルスに対処する方法を見出すための鍵である、と述べました。
コロナウイルスはみずからを複製して、細胞内に侵入するために、多くの異なるタンパク質を利用しますが、スパイクタンパク質は受容体―ヒトの細胞に侵入するための入口のような働きをするタンパク質―に結合するための鍵となる表面タンパク質です。スパイクタンパク質がヒト細胞に存在する受容体と結合すると、ウイルス膜がヒト細胞膜と融合し、ウイルスのゲノムがヒト細胞の中に侵入して、感染が始まることになります。従って、「ウイルスの吸着と融合を防ぐことが出来れば、ウイルスの細胞内への侵入を防ぐことが出来るのです」とマクレランはライブ・サイエンス(Live Science)誌上で語っています。
2019-nCoV のSタンパク質(訳注:スパイクタンパク質)の全体的な構造は、SARS-CoV のSタンパク質に似ており、959個のCα(アルファ炭素原子;訳注:タンパク質の骨格構造を構成している炭素原子のこと)の平均二乗偏差の平方根は3.8オングストロームです。これらの2つの構造の間の大きな違いの1つは(まだ比較的小さなものですが)、それぞれのダウン型立体構造におけるRBD(訳注:Receptor Binding Site、受容体結合部位)の位置です(図1)。
このような立体構造の違いが観察されたにも関わらず、2019-nCoVのSタンパク質の個々の構造ドメインがSARS-CoVのSタンパク質の対応する構造ドメインと整列している場合には、これらの構造ドメインは、2つのSタンパク質の間で、構造面において高度な相同性を有していることが示されています [1]。
この相互作用のスナップショットは、ウェストレイク先端技術研究所(Westlake Institute for Advanced Study)のチャン・ツォウ(Qiang Zhou)と彼の同僚たちが低温電子顕微鏡法を用いて撮影したものであり、血圧の制御に関与している酵素の一つであるアンギオテンシン変換酵素(Angiotensin Converting Enzyme; ACE2)をコロナウイルスが乗っ取るときに、背後で働いている化学的な仕組みの一部を明らかにしています。
研究者たちは、この構造を調べることで、この相互作用を阻止する抗体の開発に繋がる可能性があると考えています。ACE2は、アンギオテンシンというホルモンを活性型に変換する一連の酵素の中で、最初のものです。アンギオテンシンは、酵素によって切断されると、血管を収縮させます。SARS-CoV-2のスパイクタンパク質には、ヒトの細胞に感染する際に関与する2つの重要な部位があります。S1サブユニットのアミノ酸配列の一部は、ペプチド分解酵素ドメインと呼ばれるACE2のタンパク質切断部分に直接結合します。スパイクタンパク質のS2サブユニットは、ウイルスがヒト細胞に融合するのを助けます。
科学者たちは、ACE2のタンパク質切断部分が、酵素の表面に存在する橋のような構造から形成される極性相互作用を通じて、スパイクに結合することを発見しました。受容体結合ドメインの両端は、水素結合とファンデルワールス力によって、ACE2に吸着します。マクレランは、2003年にSARS(重症急性呼吸器症候群)の大流行を引き起こしたウイルスよりも、SARS-CoV-2の方が、ACE2により強く結合することができると述べています。ツォウの研究は、塩で作られた橋のような構造を作ってファンデルワールス相互作用を改善することができる微細なアミノ酸の変化が存在することを示しており、このアミノ酸の変化こそが、相互作用が強くなることの基盤となっているのではないか、とツォウは述べています [2]。
仮説
水は自然における背景のようなものであり、その中で、あらゆる生化学的なプロセスが進行しています。自然界においては、たった4種類の相互作用(強い力、弱い力、電磁気力、および重力)のみが知られています。相互作用のうちの2つは原子核のみと関係しており、重力の相互作用は宇宙的なスケールでのみ明らかになります。従って、生物学的なシステムの範囲においては、電磁気力による相互作用のみが本質的であることは明白です。単純化してみると、いかなる生物学的なプロセスであっても、その全体的な特異性は、最終的にはいくつかの特定の電磁気的な相互作用に還元することが出来ることに、私たちは気づいています。
このような訳で、水の電磁気学的な諸特性は、水自身の自己組織化や他の物質への影響力において決定的な役割を果たしており、包括的に探求していかなければなりません。これらの特性は、あらゆる生化学的および生物物理学的プロセスにおいて、一つの例外もなく常に見出されるものです。
水の電気力学的な特性における特異的な性質[第一に、非常に大きな誘電率ε(ω)]は、多くの化合物の分子が自然に解離すること、そして極めて重要な微量元素で構成された、必要不可欠なイオン組成が形成されることの原因となっています。そうでなければ、生物の多くのシステムにおいて、ごく通常の操作(特に選択的な膜輸送に関する操作など)を行うことすら不可能になってしまいます。
水の分散特性の変化は、細胞、ウイルス、生体高分子、酵素などの基本的な要素の間で、遠距離において働く相互作用に対して、(分離した電荷の間に働く静電気力や、中性の原子と分子で構成されたシステムにおける相互作用を規定するファンデルワールス型の力を修正することによって)極めて強い影響を与えることができます [5]。
SARSの主要な原因となっているコロナウイルスであるSARS-CoVは、この表面酵素に結合すると、膜融合によって肺内皮細胞の中に侵入します。この相互作用は、SARS-CoVのスパイクタンパク質によって媒介されます。この結論は、肺内皮細胞で高レベルのACE2が発現しているという最近の観察によって、さらに裏付けられています。コロナウイルスは、みずからを複製して細胞内に侵入するために、多くの異なるタンパク質を利用しますが、スパイクタンパク質は受容体―ヒトの細胞に侵入するための入口のような働きをするタンパク質―に結合するために用いる鍵となる表面タンパク質です。スパイクタンパク質がヒト細胞の受容体に結合した後、ウイルス膜はヒト細胞膜と融合し、ウイルスのゲノムがヒト細胞の中に入って、感染を開始することが出来るようになります。
スパイクタンパク質の構造的な安定性は、ファンデルワールスの弱い電気力学的な力と水素結合の間の全体的な相互作用に基づいています。融合前のスパイクタンパク質が安定しているためには、コロナウイルスによってタンパク質のスパイク鎖を形成するために必要なファンデルワールス相互作用と水素結合をサポートする特定の媒体が必要です。たんぱく質が生化学的に合成される時には、常に生体系の中に水分子が存在していることが必要なので、そのような媒体は水をベースとしたものでなければなりません。続いて起こる、融合前のスパイクタンパク質から融合後のタンパク質への移行においても、コロナウイルスがヒト細胞膜と融合するのを助けるために、正しい形への移行と橋の形成をサポートする、特定の水をベースとした媒体が必要とされます。
原子間ならびに分子間で働くファンデルワールス力は、一般には比較的短距離でのみ作用し、分子間あるいは原子間の距離の7乗に反比例します。同じ半径Rの2つの球の場合、粒子間の距離Dの関数として、相互作用エネルギーWは以下のように表されます:
ここで、ハマカー定数(Hamaker constant)A131は、材料1と媒体3の比誘電率に依存します。
式(1)は、ファンデルワールス相互作用エネルギーの値に対して、比誘電率が中程度の大きさであることに、重要な意味があることを示しています。
従って、水をベースとした媒体の電気力学的なパラメーターを変更すると、ファンデルワールス相互作用と水素結合に大きな変化がもたらされ、スパイクタンパク質鎖の適切な形成が阻害されたり、中断されたりする可能性があります。このようなシナリオは、ヒト細胞膜への吸着と融合という、コロナウイルスにおける生命の連続性を、明らかに無効化します。
コロナウイルスにおける生命の連続性を中断する可能性のある媒介物として、私たちは、変則的な電気力学的特性を備えたMRET水を推奨します。MRET水は、被験者が定期的に摂取することにより、コロナウイルスによる感染を防ぐことが出来ます。
米国のAltheaDxテクノロジー社で実施された研究によって、MRET技術によって活性化された水をベースとした培地が、遺伝的なレベルで細胞に影響を与えなかったことが確認されています;それは、正常な末梢血単核細胞(PBMC; Peripheral Blood Mononuclear Cells)の形態に対して、ポジティブな影響を与えるとともに、その生存率を高めました [6]。
MRET活性化水は、米国で特許(米国特許 #6022479)が取得された分子共鳴効果技術(MRET; Resonance Effect Technology)の助けを借りて、製造されています。MRET水活性化装置は、複合構造を備えた微細な低周波の共鳴電磁場を定常的に発生する装置です。低周波複合電磁場の発生源は、高分子化合物が特定の周波数と波長の外部電磁場に晒された時に、MRET高分子化合物(三次元のフラクタル幾何学的な基質)の線形分子グループによって形成されるナノサークルの内部で生じる集中的な電気活動です。電気伝導率と誘電率の値の大幅な減少は、MRET活性化プロセスの助けを借りて生成された活性化水の中で、比較的高度かつ長距離にわたって、水分子が動的に構造化されていることを確証するものです。
活性化水を長期にわたって保存(20℃で最大5時間まで)しても、その修正された電気力学的な特性に対して、大きな影響は生じなかったため、MRET活性化水は、30分間活性化した場合には、その変則的な特性を比較的長い時間にわたって維持する能力を持っていることが確認されました。そして、60分間活性化した場合には、30分間活性化した場合よりも、さらに高いレベルの「水の長期記憶」現象が見られることが分かりました。30分間活性化したMRET水は、72℃まで加熱した後でも、大幅に低下した誘電率と導電率が保たれることから、熱効果に対して安定していることを確認することが出来ます。
このことは、極めて低い周波数範囲の電磁場に暴露されたMRET水の電気力学的な特性(誘電率と電気伝導率)が、変則的な振る舞いを見せることを示しており、MRET活性化水の偏光配向性の多層にわたる構造化と、生体系における適切な細胞機能に対するMRET水の可能な効果に関する証拠を提供してくれています。
仮説の証明
重症急性呼吸器症候群(SARS)は、発熱性の呼吸器疾患です。この疾患は、病因学的な見地から見ると、SARS関連コロナウイルス(SARS-CoV)と名付けられた新規のコロナウイルスと関連しています。このSARS-CoVのゲノムは、最近その配列が決定されたところです。それはコロナウイルス科に所属しているため、そのスパイクタンパク質(S2)は、ウイルス膜と宿主の細胞膜との間の融合を促進することによって、ウイルスが侵入する際に中心的な役割を果たしていると考えられています。
HIV-1(gp41)ウイルスによって誘発される膜融合に関与するタンパク質は、長さが異なっており、S2との間に配列の相同性はありません。多くのエンベロープウイルスが感染するためには、ウイルス膜と細胞膜の間の融合が必要です。ウイルスのエンベロープタンパク質は、この膜融合プロセスを仲介します。これらのタンパク質は、前駆体(レトロウイルス科ではENV、コロナウイルス科ではE2)として合成され、後の段階で、ウイルス誘発性の膜の融合に関与する膜貫通サブユニット(レトロウイルスHIV-1ではgp41、コロナウイルスSARS-CoVではS2)と、細胞の受容体との間の相互作用に関与する表在性のサブユニットへと加工されます。この研究は、2つのウイルスタンパク質が同様の作用機序を持っていることを示しており、ウイルスによって誘導される膜融合の段階を標的とする抗ウイルス戦略を、HIV-1からSARS-CoVへと適応させることができる、ということを示唆しています(図2)。
最近FDAは、HIV-1のgp41のC末端に存在する7残基反復配列(heptad repeat)に対応する合成ペプチドであるエンフビルチド(Enfuvirtide)を、抗エイズ薬として承認しました。エンフビルチドと、もう一つの抗HIV-1ペプチドであるC34は、gp41のロイシンジッパーもしくはイソロイシンジッパー様の配列に結合して、活性化に必要なgp41の構造変化を阻止することによって、阻害活性を発揮します。私たちは、S2タンパク質のC末端の7残基反復配列に対応するペプチドが、SARS-CoVの侵入に対する阻害剤として働いている可能性を示唆しています [3]。
図2 HIV-1とSARS-CoVの融合タンパク質の間の類似性。HIV-1 gp41(a)およびSARS-CoVにおいて同等の働きをしているS2タンパク質(b)が示されています。両方のタンパク質のN末端に隣接するロイシン/イソロイシンの7残基反復配列が赤色で表示されています。C末端の7残基反復配列は緑色で示されています。ループ構造を構築するシステイン残基(紫色)は、2つの7残基反復配列の間にあります。芳香族残基が豊富なモチーフは青色でマークされ、膜貫通セグメントは橙色で示されています。HIV-1の細胞内への侵入に対して、強力な阻害剤として作用するC末端の7残基反復配列に対応するペプチドは、黄色で表示されています [3]。
タイのロッブリー県(Lopburi Province)のワット・プラバートナンプ(Wat Phra Baht Nam Phu)にあるThammarakniwet財団で、臨床観察が行われました。調査は、バンコク首都圏のエイズ対策局長であるペラヨット・トロンサワド(Peerayot Trongsawad)医学博士の監督の下で行われました。
この研究は、2004年8月から2005年8月まで、38人のエイズ患者を対象に実施されました。すべての患者は、抗HIV薬の処方に加えて、無料の治療として1日あたり1.5リットルのMRET活性化水を摂取しました。臨床観察の過程では、38人の患者全員に対して、定期的にCD4細胞の数が測定され、患者は健康状態に関するレポートを毎週、提出することになりました。
同じ期間中に、別のエイズ患者群に対して、同時に観察が行われました(対照群)。彼らには同じタイプの抗HIV薬が処方されましたが、無料のMRET水は与えられませんでした [4]。
第一の方法:毎週の健康状態に関するレポートとCD4細胞の計数に関するレポートの収集と分析。
第二の方法:この観察に参加した患者へのグループインタビューと個人インタビュー。
19歳から49歳までの年齢の38人の患者が、臨床試験のために選ばれました。
観察結果を要約しますと、調査対象であるエイズ患者の健康状態の変化に従って、36人の患者が有意な健康状態の改善を示しましたが、2人の患者の健康状態は改善しませんでした。
予算が制限されているために、2人の患者が選ばれて、バンコク病理学研究所で2つの検査を受けることになりました。1つのテストはCD4細胞(免疫系)の計数であり、もう1つはウイルス負荷(体内のウイルス量)でした。CD4細胞の計数においては、健康な体の場合には、1マイクロリットル当たり800〜1,200細胞になっているはずです。
ウイルス負荷の場合、装置には1ミリリットル当たり50~5,000コピーを測定する能力があります。数値が低ければ低いほど、体内のウイルス量は少なくなり、患者の体への攻撃も少なくなります。
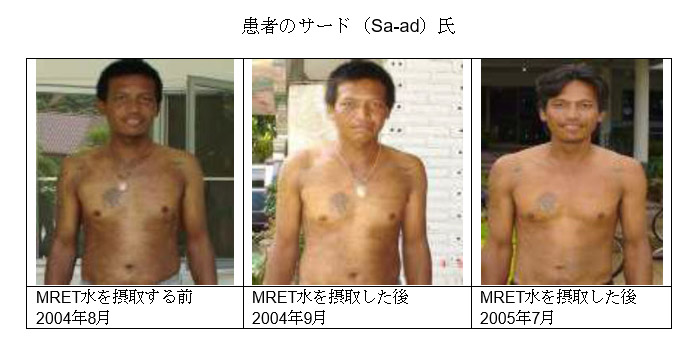
一人目の患者、サード氏(Mr. Sa-ad):
彼のCD4細胞の数は、MRET活性化水の摂取を開始してから11か月以内に、2から840まで増加しました。彼のウイルス負荷は50未満でした。
二人目の患者、ウン・ルアング氏(Mr. Un-ruang):
彼のCD4細胞の数は、MRET水の摂取を開始してから3か月以内に、90から805へと増加しました。彼のウイルス負荷もまた50未満でした。
MRET水の摂取をしなかった患者グループ:
MRET水を摂取しなかった患者たち(対照群)を同時に観察した結果、これらの患者は、健康状態の有意な改善をまったく示さなかった、という証拠を得ることが出来ました。
結論
2004年から2005年にかけて、タイのロッブリー県のワット・プラバートナムプにあるThammarakniwet 財団で行われた臨床試験において、HIV患者に対するMRET水の摂取による無料治療によって、ポジティブな結果が得られたことを観察しました。最近の研究データによれば、2つのウイルスタンパク質がよく似た作用機序を示すことが指摘されてきており、ウイルスによって誘導される膜融合のステップを標的とする抗ウイルス戦略が、HIV-1からSARS-CoVへと適応出来ることが示唆されています。
患者によるMRET水の摂取は、誘電率、電気伝導率、および人体の水をベースとした媒体における水素結合の変化につながる可能性があることが示唆されています。それはファンデルワールス相互作用と水素結合に大きな変化をもたらし、それらが変化したことの結果として、ウイルスのスパイクタンパク質鎖の適切な形成の阻害と中断が起こります。このようなシナリオは、ヒト細胞膜への付着と融合というコロナウイルスの生命の連続性を明らかに無効化します。
文献
[1] Daniel Wrapp, Nianshuang Wang, Kizzmekia S. Corbett,, Jory A. Goldsmith, Ching- Lin Hsieh1 Ching-Lin Hsieh, , Olubukola Abiona, Barney S. Graham, Jason S. McLellan, «Cryo-EM structure of the 2019-nCoV spike in the pre-fusion conformation», Science 13 Mar 2020: Vol. 367, Issue 6483, pp. 1260-1263.[2] Megha Satyanarayana, «Researchers in China report structure of the novel coronavirus bound to its human target». Biochemistry, March 6, 2020.
[3] Yossef Kliger, Erez Y Levanon, «Cloaked similarity between HIV-1 and SARS-CoV suggests an anti-SARS strategy», BMC Microbiol. 2003; 3: 20.
[4] Igor Smirnov, Peerayot Trongsawad, «The Clinical Observation of MRET Activated Water Effect on Patients Suffering from AIDS», Asian J. Exp. Biol. Sci. Vol. 1 (3) 2010.
[5] Vladimir Vysotskii, Alla Kornilova, Igor Smirnov, “Applied Biophysics of Activated Water: The Physical Properties, Biological Effects and Medical Applications of MRET Activated Water”, World Scientific Pub Co Inc (July 12, 2009), ISBN-10: 9814271187; ISBN-13: 978-9814271189.
[6] Igor Smirnov, «The comparative analysis of the effect of MRET treatment on morphology of HeLa cancer cells and PBMC normal cells», Am. J. Sci. Ind. Res., 2010, 1(1): 25-28.
 イゴール・スミルノフ博士
イゴール・スミルノフ博士
原子核工学を学んでサンクトペテルブルク海軍アカデミーを卒業。同アカデミーで、機械工学とバイオ工学の両分野で科学の修士号を取得。さらにサンクトペテルブルク州立大学で、臨床心理学の分野で博士号を取得。「MRET(分子共鳴効果技術)」の開発者として広く知られている。低周波電磁波の人間の細胞生理に及ぼす影響に関する研究におけるスペシャリストでもある。
